-
業種・地域から探す
めっき技術(2023年12月)
金属イオン種を含む溶液を電解して物質を析出させる電析・電気めっきでは、めっき浴の設計が技術開発のポイントとなる。水溶液系の電気めっきには、濃度1モル/リットル程度の溶質(金属塩、支持塩、配位子など)を含む浴を使うことが多いが、さらに濃度が高い浴を設計することで、これまでにない電析・電気めっきが可能になり、世界初となる水溶液系の硬質3価クロムめっきなどへと展開されている。このような浴では、副反応の水素発生が抑制されたり、希薄な濃度条件では安定でない金属錯体が生じる。
濃厚・超濃厚水溶液を活用する電析技術
水和物融体を使う金属電析 環境配慮技術として期待
-
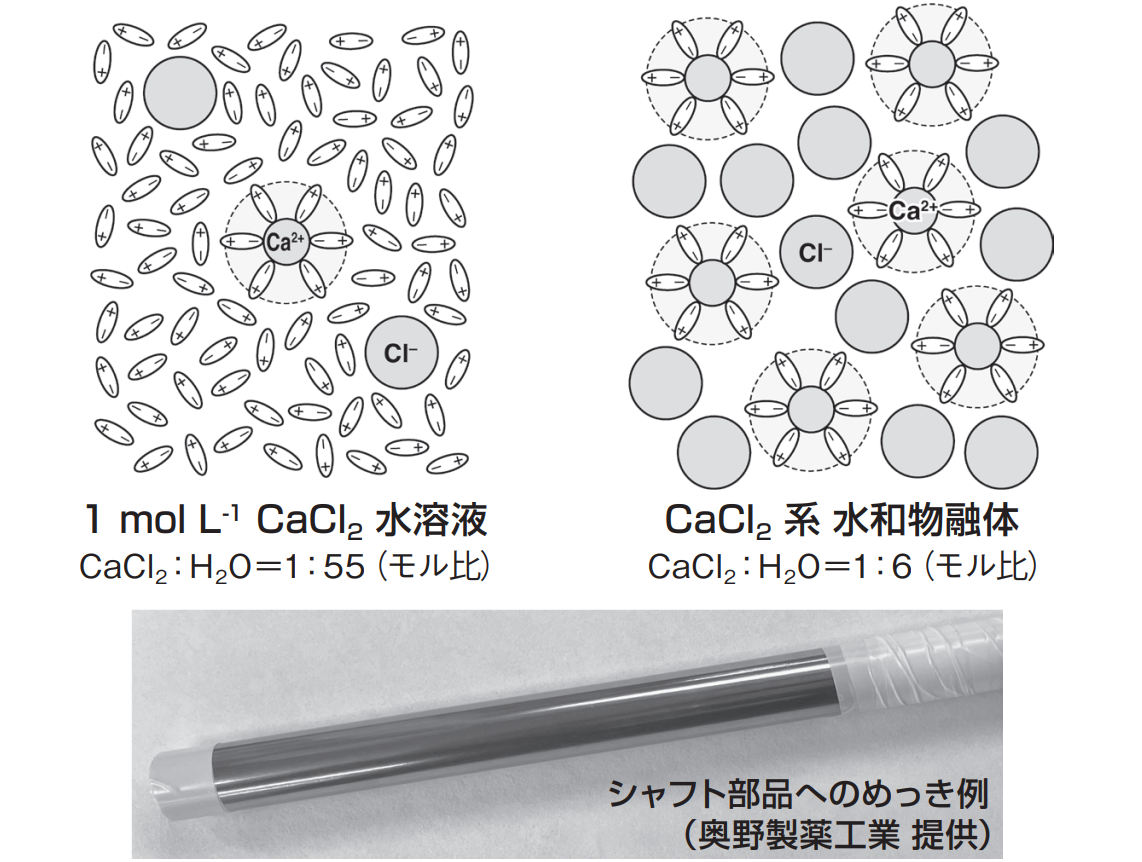
図1 濃度の異なる塩化カルシウム水溶液に含まれる化学種の様子(楕円は水分子を表す)と、水和物溶融体を用いた硬質3価クロムめっきの試作品写真
例えば、塩化カルシウム六水和物は、約30度C以上の温度で融解して液体となる。この状態は水和物融体(ハイドレートメルト)と呼ばれ、いわば塩化カルシウムの超濃厚水溶液である。その濃度を容量モル濃度で表せば6・8モル/リットルになるが、このような高濃度まで室温で水に溶かすことができる金属塩は実は少なく、他に塩化リチウムや酢酸カリウムなどが知られる。
筆者のグループでは、塩化物系の水和物融体を新しい水系の「溶媒」と考え、電析・電気めっきへの応用を研究している。図1は(左)濃度1モル/リットルの塩化カルシウム水溶液と、(右)塩化カルシウム六水和物の水和物融体の模式図である。
一般的な塩濃度の前者では、水分子は一部がイオン(主として陽イオン)へと水和した状態にあるものの、それを除くほとんどはイオンとの相互作用がないフリーな水(自由水)として存在している。
これに対し、水和物融体に含まれる水分子はイオンへの水和に使い尽くされ、結果として自由水は枯渇している。(水和した)陽イオンと陰イオンのみからなる状況では、イオン同士の静電的な相互作用が大きくなり、その結果、水和物融体の粘性は一般的な水溶液よりもいくぶん大きくなって、電析過程で必要な電解液中のイオン移動は制約を受ける。
しかし、このいくぶん高い粘性が、金属の平滑な電析に対して効果的にはたらく場合がある。また、自由水の少なさは水の有効濃度(活量)の小ささを意味する。自由水が少なければ、それを足場として溶液中を移動する水素イオンの動きも遅くなる。
これらの効果によって、卑な金属を電析する際に副反応となる水素発生が起こりにくくなり、金属電析の電流効率が高まる。さらに、高い塩化物イオン濃度が金属塩の溶解性に効果をおよぼすことがある。通常、塩化銀や塩化鉛は水溶液に対して難溶だが、塩化物イオン濃度が著しく大きな環境では塩化物錯体を生成し、逆に溶解性が高まる。
塩化銀を塩化カルシウム系の水和物融体へ溶解させためっき液を使い、銅素地への銀の置換めっきを試みたところ、硝酸銀水溶液を使った置換めっきに比べて平滑なめっきが可能とわかった。シアンフリーの置換銀めっき液として期待される。同様に塩化鉛を水和物融体へ加え、鉛電析に使うこともできる。
鉛は、硫酸塩や塩化物が水に難溶なため、工業的な鉛電解製錬ではケイフッ酸浴が使われ、フッ化水素や四フッ化ケイ素の揮発による環境汚染や含フッ素排液の処理が課題である。塩化鉛と水和物融体を用いた浴は、鉛イオンの溶解上限がケイフッ酸浴の6分の1程度しかない欠点はあるが環境に優しい鉛電析浴として期待される。
3価の塩化クロムを水和物融体へ加えためっき浴からは、結晶性の硬質クロムめっき厚膜が最大80%の高い電流効率で析出する。これは現行の6価クロム浴に代わる世界初の工業用3価クロムめっきとして期待され、現在、奥野製薬工業において実製品への展開が検討されている。
錯体とめっきの相関を知る 亜酸化銅電析浴中の化学種を解明
-
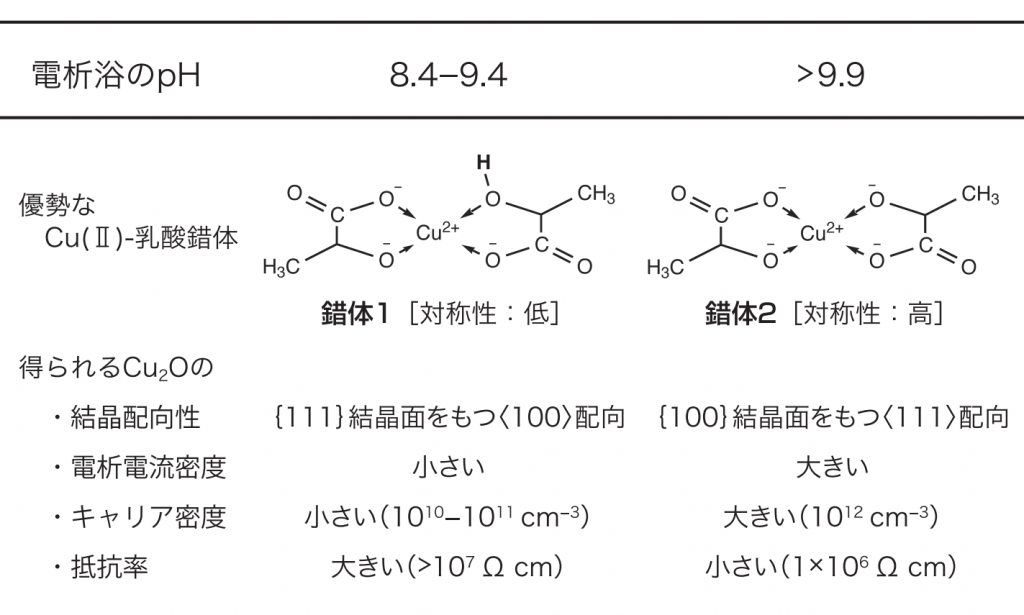
図2 濃厚な乳酸を含むアルカリ性の銅(Ⅱ)―乳酸浴において安定な二つの錯体種とそこから得られる亜酸化銅薄膜の性質
亜酸化銅(Cu2O)はバンドギャップ2・1電子ボルト(eV)のp型半導体である。資源的に豊富なコモンメタルの酸化物であることから、安く環境負荷の少ない半導体材料として太陽電池や光電極への応用研究が進んでいる。
亜酸化銅の薄膜をめっき技術でつくる研究は多く、35年以上の歴史をもつ。ここでは濃度0・4モル/リットルの銅(Ⅱ)塩に対し、3モル/リットルの乳酸イオン含むアルカリ性の浴が連綿と使われてきた。このとき銅(Ⅱ)イオンは乳酸イオンと錯体を形成しているが、銅(Ⅱ)イオンに対する乳酸イオンの濃度(7・5倍)は通常の錯形成に比べてかなり過剰に思える。
しかし、興味深いことに銅(Ⅱ)イオンに対する乳酸イオンの濃度を下げたり、銅(Ⅱ)イオン/乳酸イオンの濃度比を保ったまま全体的に希釈したりすると、アルカリ性領域では建浴できず、水酸化銅が沈殿してしまう。すなわち、乳酸イオンが濃厚な溶液環境を用意することで浴が安定に保たれており、このときどのような銅(Ⅱ)―乳酸錯体が生じているのか不明であった。
筆者のグループは滴定曲線の解析、電子スペクトルの多変量解析、ならびにエレクトロスプレー質量分析を組み合わせ、濃厚な乳酸環境のアルカリ性の浴に含まれる銅(Ⅱ)―乳酸錯体が図2に示す二つであることを明らかにし、錯生成定数を決定した。また、建浴の際、水素イオン指数(pH)をアルカリ性に調整したあと、安定した銅(Ⅱ)―乳酸錯体となるまでに一定の時間を要することを、電子スペクトルの経時変化から見いだした。
アルカリ性の銅(Ⅱ)―乳酸浴を用いる亜酸化銅の電析では、pH9・5付近を境に、得られる薄膜の電気的性質や結晶配向性が互いに異なることが実験的に知られる。錯生成定数が決まり、亜酸化銅析出の熱力学的な平衡電位が求まったことを機に、アルカリ性領域の種々のpHをもつ銅(Ⅱ)―乳酸浴を1日かけて十分に安定化させて建浴し、過電圧を統一した電析試験を行って得られる亜酸化銅を比較した。
その結果、物性の境界となるpH9・5は、浴における優勢な銅(Ⅱ)―乳酸錯体(錯体1と錯体2)の境界にほぼ一致することがわかった(図2)。より対称性の高い錯体2からの電析では、銅(Ⅱ)イオンの結晶への組み込みが速度論的に遅れ、p型半導体としての性質を決める銅(Ⅱ)イオンの欠損が生じやすいことが理由と考えられる。
【執筆】
京都大学工学研究科 教授 邑瀬 邦明
東京大学工学系研究科 准教授 北田 敦

